Սանկտ Պետերբուրգի պետական \u200b\u200bտեխնոլոգիական ինստիտուտ
(Տեխնիկական համալսարան)
Օրգանական քիմիայի ֆակուլտետի ֆակուլտետ 4
476 խումբ:
Դասընթացի աշխատանքներ
Ալկենեսի օքսիդացում
Ուսանող ............................................. Rytin A.I.
Դասախոս .................................... ... Սանկտ Պետերբուրգ Յու.Լ.
Սանկտ Պետերբուրգ
Ներածություն
1.Poxidation (արձագանք N.A. Prilezhev, 1909)
2. Հիդրոքսիլիզացում
2.1հակա -Հիդրոքսիլացիա
2.2կար -Հիդրոքսիլացիա
3. Ալկենեսի օվկիչով պառակտում
4. Պարբերաբար
5. Ալկենեսի հասարակությունը պալադիումի աղերի ներկայությամբ
Եզրակացություն
Օգտագործված աղբյուրների ցուցակ
Ներածություն
Օքսիդացումը օրգանական միացությունների ամենակարեւոր եւ ընդհանուր վերափոխումներից մեկն է:
Օրգանական քիմիայի օքսիդացման ներքո, այն գործընթացները, որոնք հանգեցնում են ջրածնի կամ հարստացմանը իր թթվածնով: Այս դեպքում տեղի է ունենում էլեկտրոնի մոլեկուլ: Ըստ այդմ, վերականգնումը հասկանում է օրգանական թթվածնի մոլեկուլից տարանջատումը կամ ջրածնի կցորդը դրան:
Օքսիդացուցիչի նվազեցման ռեակցիաներում օքսիդացուցիչները միացություններ են `էլեկտրոնի (էլեկտրոֆիլա) եւ գործակալների նվազեցման համար մեծ կապ ունեցող միացություններ` միացություններ, որոնք էլեկտրոններ (նուկլեոֆիլներ վերադարձնելու հակում ունեն: Բաղադրության օքսիդացման հեշտությունը մեծանում է իր նուկլեության աճով:
Օրգանական միացությունները օքսիդացնելիս, որպես կանոն, էլեկտրոնների ընդհանուր փոխանցումը եւ, համապատասխանաբար, ածխածնի ատոմների վալենտի փոփոխությունները չեն առաջանում: Հետեւաբար, օքսիդացման աստիճանի հայեցակարգը մոլեկուլում ատոմի պայմանական մեղադրանքն է, որը հաշվարկվում է, հիմնվելով այն ենթադրության վրա, որ մոլեկուլը միայն իոններից բաղկացած է միայն պայմանական, ձեւական բնույթ:
Redox ռեակցիաների հավասարումների պատրաստման ժամանակ անհրաժեշտ է որոշել նվազեցնող գործակալը, օքսիդացնող գործակալը եւ նվիրված եւ ստացված էլեկտրոնների քանակը: Որպես կանոն, գործակիցներն ընտրվում են էլեկտրոնային ION հաշվեկշռի մեթոդով (կիսաշրջանի ձեւավորման մեթոդ):
Այս մեթոդով էլեկտրոնների անցումը մեկ ատոմներից կամ իոններից մյուսը, հաշվի առնելով միջոցի (թթվի, ալկալային կամ չեզոք) բնույթը, որում իրականացվում է ռեակցիան: Երկրպագել թթվածնի եւ ջրածնի ատոմների կամ ջրի մոլեկուլների եւ պրոտոնների քանակը (եթե թթու միջին) կամ ջրի մոլեկուլներն ու հիդրօքսիդի իոնները (եթե ալկալին) ներդրվի:
Այսպիսով, վերականգնման եւ օքսիդացման սեմիտներ գրելիս անհրաժեշտ է ելնել իոնների կազմից, որոնք լուծման մեջ են: Գազի տեսքով թողարկված չարագործությունները, վատ լուծելի կամ գազը պետք է գրվեն մոլեկուլային ձեւով:
Որպես օրինակ հաշվի առեք էթիլենային օքսիդացման գործընթացը կալիումի permanganate- ի նոսր ջրային լուծույթով (Վագների ռեակցիա): Այս արձագանքի ընթացքում էթիլենը օքսիդացվում է էթիլեն գլիկոլի վրա, եւ կալիումի պերմանգանատը վերականգնվում է մանգան երկօքսիդին: Կրկնակի կապի ժամանակ երկու հիդրոքսիլ է միանում.
3C 2 H 4 + 2KMNO 4 + 4H 2 O → 3C 2 H 6 O 2 + 2MNO 2 + 2KOH
Կիսա-ռեակցիայի վերականգնում. MNO 4 ¯ + 2H 2 O + 3 Ե. → Mno 2 + 4oh ¯ 2Օքսիդացման կիսաեզրափակիչ. C 2 H 4 + 2OH - - 2 Ե. → C 2 H 6 O 2 3
Վերջապես մենք ունենք իոնային տեսքով.
2MNO 4 ¯ + 4H 2 O + 3C 2 H 4 + 6OH ¯ → 2MNO 2 + 8OH + 3C 2 H 6 O 2
Նման անդամների անհրաժեշտ կրճատումներն իրականացնելուց հետո գրել հավասարումը մոլեկուլային ձեւով.
3C 2 H 4 + 2KMNO 4 + 4 H 2 O \u003d 3C 2 H 6 O 2 + 2MNO 2 + 2KOH.
Բնորոշ որոշ օքսիդացնող գործակալների
Թթվածին
Օդային թթվածինը լայնորեն օգտագործվում է տեխնոլոգիական գործընթացներում, քանի որ դա ամենաէժան օքսիդիչն է: Բայց օդային թթվածնի թթվածնի թթվածնումը կապված է գործընթացի վերահսկողության հետ կապված դժվարությունների հետ, որոնք հոսում են տարբեր ուղղություններով: Օքսիդացումը սովորաբար իրականացվում է բարձր ջերմաստիճանում կատալիզատորների ներկայությամբ:
Օզոն
Ozone O 3-ը օգտագործվում է Aldehydes եւ Ketones ձեռք բերելու համար, եթե դրանք դժվար է ձեռք բերել այլ եղանակներով: Ամենից հաճախ օզոնը օգտագործվում է չհագեցած միացությունների կառուցվածքը հաստատելու համար: Օզոնը ձեռք է բերվում թթվածնի վրա հանգիստ էլեկտրական լիցքաթափման գործողությամբ: Օզոնիզացման զգալի առավելություններից մեկը, քլորացման հետ համեմատ, վերամշակումից հետո տոքսինների բացակայությունն է:
Կալիումի permanganate
Permanganate կալիումը առավել հաճախ օգտագործվում է օքսիդացնող միջոց: Re ակատը ջրի մեջ լուծելի է (6.0% 20 ° C- ում), ինչպես նաեւ մեթանոլում, ացետոն եւ քացախաթթու: Օքսիդացման, ջրային (երբեմն ացետոն) լուծումներ KMNO 4-ը չեզոք, թթու կամ ալկալային միջավայրում օգտագործվում են: Չեզոք միջավայրում գործընթաց իրականացնելիս մագնեզիումը, ալյումինը կամ ածխաթթու գազը ավելացվում է կալիումի թողարկված հիդրօքսիդի չեզոքացման մեջ, ավելացվում է ռեակցիայի զանգվածին: KMNO 4-ի օքսիդացման արձագանքը թթվային միջավայրում առավել հաճախ իրականացվում է ծծմբաթթվի առկայության դեպքում: Օքսիդացման ալկալային միջավայրը ստեղծում է ռեակցիայի ընթացքում առաջացած KOH- ն, կամ այն \u200b\u200bի սկզբանե ավելացվում է ռեակցիայի զանգվածին: Թույլ ալկալային եւ չեզոք մեդիա, KMNO 4 օքսիդացնում է հավասարումը.
KMNO 4 +. 3 Ե. + 2H 2 O \u003d k + + MNO 2 + 4OH
Թթվային միջավայրում.
KMNO 4 +. 5 Ե. + 8h + \u003d k + + MN 2+ + 4H 2 O
Կալիումի Permanganate- ը օգտագործվում է Ալկենեսից 1,2 դիոլներ ձեռք բերելու համար, առաջնային ալկոհոլների, ալդեհիդների եւ ալկիլարների օքսիդացումով, ինչպես նաեւ ածխածնի կմախքի օքսիդացնող պառակտման համար բազմաթիվ պարտատոմսերի միջոցով:
Գործնականում սովորաբար օգտագործվում է բավականին մեծ ավելցուկ (ավելի քան 100%) KMNO 4: Սա բացատրվում է այն փաստով, որ նորմալ պայմաններում KMNO 4-ը մասամբ քայքայվում է Manganese երկօքսիդի վրա, O 2-ի թողարկմամբ: Քայքայված խտացված H 2 Այսպիսով, երբ ջեռուցվում է պայթյունի հետ վերակառուցվածքի առկայության դեպքում. Պայթուցիկ նյութեր են նաեւ կալիումի պերմանգանատի խառնուրդները օրգանական նյութերով:
Նադկիսլոտ
Peracetic եւ permaraye թթուները ձեռք են բերվում 25-90% ջրածնի պերօքսիդի արձագանքով համապատասխան կարբոքսային թթվով `համաձայն հետեւյալ արձագանքի.
Rcooh + h 2 o 2 \u003d rcoooh + h 2 o
Քացետիկ թթվի դեպքում այս հավասարակշռությունը սահմանվում է համեմատաբար դանդաղ, եւ գագաթների ձեւավորումը արագացնելու համար սովորաբար ածուխի թթու է ավելացնում: Ձեւաթթվին ինքնուրույն բավականաչափ ուժեղ է, որպեսզի ապահովվի հավասարակշռության արագ հաստատումը:
Պրեպոֆոնտուզի թթու, որը ձեռք է բերվել խառնուրդով, տրիֆլյուլեկտորական անհեթեթության ռմբակոծելի ռեակտիվի հետ, 90% ջրածնի պերօքսիդով, նույնիսկ ավելի ուժեղ օքսիդացուցիչով: Նմանապես, Պերոքթուն թթու կարելի է ձեռք բերել քացախային անհիդրիդ եւ ջրածնի պերօքսիդ:
Հատկապես հանրաճանաչ ֆիրման Տղամարդ -Հլորբենզուաթթու, քանի որ այն համեմատաբար անվտանգ է շրջանառության մեջ, այն բավականին կայուն է եւ երկար ժամանակ կարող է պահվել:
Օքսիդացումը տեղի է ունենում թողարկված թթվածնի ատոմի պատճառով.
Rcoooh \u003d rcoh + [o]
Nadcisitles- ը օգտագործվում է Ալիկիկլիկ Կետոններից, ինչպես նաեւ լակտոններից `էպոքսես-ից:
Ջրածնի պերօքսիդ
Hyd րածնի պերօքսիդը անգույն հեղուկ է, խառնված ջրի, էթանոլի եւ դիէթիլային էթերի հետ: 30% լուծույթ H 2 O 2-ը կոչվում է perhydro: Խիստ կենտրոնացած դեղը կարող է արձագանքել օրգանական նյութերով `պայթյունով: Երբ պահում է քայքայվել թթվածնի եւ ջրի վրա: Ջրածնի պերօքսիդի դիմադրությունը մեծանում է նոսրացման հետ: Օքսիդացման համար օգտագործվում են տարբեր կոնցենտրացիաների ջրային լուծումներ (3-ից 90%) չեզոք, թթվային կամ ալկալային լրատվամիջոցներում:
H 2 O 2 \u003d H 2 O + [o]
Այս ռեակտիվի action α, β-ինհավաքաբրված կարբոնիկ միացություններում ալկալային միջավայրում ստացվում են համապատասխան epoxyaldehydes եւ ketones, թթվային միջավայրում կարբոքսիլային թթուների օքսիդացում սինթեզված է: Acetic թթվի 30% լուծույթ H 2 O 2-ը օքսիդացնում է Ալկենեսը 1,2-դիով: Օգտագործվում է ջրածնի պերօքսիդը. Օրգանական եւ անօրգանական պերօքսիդներ, խճանկար եւ պերկարբոնատ ԱԺ; Որպես հրթիռային վառելիքի օքսիդացնող միջոց; Tyurama et al- ի խմբի խմբի, էթօքսիոն, պիրոկատեխինի, էթօջախների, բիկիկոլի, էթիլեն գլիկոլիացման արագացման պատրաստման նախապատրաստման մեջ; յուղերի, ճարպերի, մորթեղենի, կաշվե, տեքստիլ նյութերի, թղթի համար; Գերմանիայի եւ սիլիկոնային կիսահաղորդչային նյութերի մաքրման համար. Որպես կենցաղային եւ արդյունաբերական կեղտաջրերի տրամադրման ախտահանիչ. բժշկության մեջ; որպես սուզանավում 2-ի աղբյուր; H 2 O 2-ը Fenton Reagent (Fe 2 + H 2 O 2) մաս է, որն օգտագործվում է որպես օրգանական սինթեզում անվճար ռադիկալների աղբյուր:
Ruthenium Tetraxides եւ Osmia
Tetraoxide Osmia OSO 4 - փոշի սպիտակից մինչեւ գունատ դեղին գույնը տ. Պ. 40.6ºС; տ. Կիպ: 131.2ºС. Այն հանվում է սենյակային ջերմաստիճանում, ջրի մեջ լուծելի (7.47 գ 100 մլ 25 ° C ջերմաստիճանում), CCL 4 (250 գ 100 գ լուծիչ 20 ° C): Օրգանական միացությունների առկայության դեպքում, դարբին, Օսո 2-ի վերականգնման պատճառով:
Ruo 4-ը Golden Yellow Prism է T- ով: PL. 25.4ºс, նկատելիորեն իրականացվում է սենյակային ջերմաստիճանում: Չափավոր լուծելի ջրի մեջ (2.03 գ 100 մլ 20 ° C- ով), շատ լավ լուծելի CCL 4-ում: Ուժեղ օքսիդիչ, քան OSO 4: 100ºС-ից բարձր պայթում է: Ինչպես նաեւ OSMIUM Tetraoxide- ն ունի մեծ թունավորություն եւ բարձր գին:
Այս օքսիդացուցիչները օգտագործվում են ալկետիկների օքսիդացման համար `մեղմ պայմաններում:
Այս նյութը կարող է ծալվել ինքնուրույն ուսումնասիրության մեջ, մեծ քանակությամբ տեղեկատվության, բազմաթիվ նրբություններ, բոլոր տեսակի, բայց եթե: Կարդացեք ուշադիր:
Ինչի մասին ենք խոսելու:
Բացի օքսիդացումից (այրումը), օրգանական միացությունների որոշ դասերի համար բնութագրվում է թերի օքսիդացման արձագանքը, մինչդեռ դրանք վերածվում են այլ դասերի:
Յուրաքանչյուր դասի համար կան հատուկ օքսիդիչներ, CUO (ալկոհոլի համար), CU (OH) 2 եւ OH (Aldehydes) եւ այլն:
Բայց կան երկու դասական օքսիդիչներ, որոնք, եթե այդպես է, արտահայտվում են, համընդհանուր շատ դասերի համար:
Սա կալիումի permanganate է `KMNO 4: Եւ կալիումի երկկողմանի (երկիմատ) - k 2 cr 2 o 7: Այս նյութերը ուժեղ օքսիդացուցիչներ են, որոնք մանգանում են մանգանի միջոցով օքսիդացման աստիճանի +7, եւ քրոմը `համապատասխանաբար օքսիդացման աստիճանի +6:
Այս օքսիդացուցիչների հետ արձագանքները բավականին հաճախ են հայտնաբերվում, բայց ոչ մի տեղ չկա ամբողջական ղեկավարություն, ըստ որի սկզբունքը ընտրում է նման ռեակցիաների արտադրանք:
Գործնականում կան բազմաթիվ գործոններ, որոնք ազդում են ռեակցիայի ընթացքի վրա (ջերմաստիճանը, միջին, ռեակտիվների կենտրոնացումը եւ այլն): Հաճախ այն ստացվում է ապրանքների խառնուրդ: Հետեւաբար, կանխատեսել այն արտադրանքը, որը ձեւավորվում է գրեթե անհնարին:
Եվ քննության համար հարմար չէ. Անհնար է գրել «գուցե կամ այդպես, կամ այլ կերպ, կամ այլապես արտադրանքի խառնուրդ»: Անհրաժեշտ է հատուկ:
Առաջադրանքի կազմողները ներդրել են որոշակի տրամաբանություն, որի որոշակի սկզբունք պետք է գրել որոշակի ապրանք: Դժբախտաբար, նրանք ոչ մեկի հետ չէին կիսում:
Օգուտների մեծ մասում այս հարցը բավականին սայթաքում է կուսակցության կողմից. Երկու կամ երեք ռեակցիա տրվում է որպես օրինակ:
Ներկայացնում եմ այս հոդվածում, ինչը կարելի է անվանել օգտագործման առաջադրանքների հետազոտության արդյունքները: Օքսիդացման ռեակցիաների պերմանգանատ եւ համերաշխության ռեալարիայի կազմի տրամաբանությունն ու սկզբունքները բավականին բարձր ճշգրտություն են (ըստ օր. Ստանդարտների): Ամեն ինչի մասին:
Օքսիդացման որոշում.
Առաջինը, երբ մենք գործ ունենք Redox Reactions- ի հետ, միշտ կա օքսիդացնող գործակալ եւ նվազեցնող միջոց:
Oxidizer- ը Permanganate- ի կամ Chrome- ի մանգան է, որը գտնվում է օրգանական (մասնավորապես, ածխածնի ատոմներում):
Փոքր ապրանքները հայտնաբերելու համար արձագանքը պետք է հավասարեցվի: Ճշգրտման համար ավանդաբար օգտագործեք էլեկտրոնային մնացորդի մեթոդը: Այս մեթոդը կիրառելու համար անհրաժեշտ է որոշել ռեակցիայի առաջ եւ հետո առաջ եւ հետո օքսիդիչների օքսիդացման օքսիդացման աստիճանը:
Օքսիդացման աստիճանի անօրգանական նյութերը կարող են կարողանան 9-րդ դասարան.
Բայց կազմակերպման ժամանակ, հավանաբար, 9-րդ դասարանում որոշված \u200b\u200bչէին: Հետեւաբար, նախքան սովորելը, թե ինչպես գրել OSR- ը օրգանական քիմիայում, դուք պետք է սովորեք, թե ինչպես որոշել օրգանական նյութերի ածխածնի օքսիդացման աստիճանը: Դա արվում է մի փոքր այլ կերպ, այլապես, քան անօրգանական քիմիայի մեջ:
Ածխածինը ունի օքսիդացման առավելագույն աստիճան + 4, նվազագույն -4: Եվ դա կարող է ցուցադրել այս բացի օքսիդացման ցանկացած աստիճան. -4, -3, -2, -1, 0, +1, +2, +4, +4:
Նախ պետք է հիշել, թե որն է օքսիդացման աստիճանը:
Օքսիդացման աստիճանը ատոմի վրա բխող պայմանական մեղադրանք է, երբ ենթադրում է, որ էլեկտրոնային զույգերը ամբողջովին տեղափոխվում են ավելի շատ էլեկտրական ատոմ:
Հետեւաբար, օքսիդացման աստիճանը որոշվում է տեղահանված էլեկտրոնային զույգերի քանակով. Եթե այն տեղափոխվում է այս ատոմը, այն ձեռք է բերում ավելորդ մինուս (-) լիցք, եթե ատոմից ստացվի, ապա այն ստանում է ավելորդ գումարած (+) գանձում: Սկզբունքորեն, սա այն ամբողջ տեսությունն է, որը դուք պետք է իմանաք, որ որոշեք ածխածնի ատոմի օքսիդացման աստիճանը:
Միացության մեջ որոշակի ածխածնի ատոմի օքսիդացման աստիճանը որոշելու համար մենք պետք է հաշվի առնենք յուրաքանչյուր կապ եւ տեսեք, թե որ ուղղությամբ է կտեղափոխվեն էլեկտրոնի գոլորշին, եւ որ ավելորդ լիցքը (կամ -) արդյունքի կհանգեցնի ածխածնի ատոմում:
Մենք կվերլուծենք հատուկ օրինակներ.
Ածխածին Երեք կապ `ջրածնի հետ, Ածխածնի եւ ջրածնի - ով է ավելի շատ էլեկտրաէներգիա: Ածխածնի, դա նշանակում է, որ այս երեք պարտատոմսերը էլեկտրոնային զույգը կտեղափոխվի դեպի ածխածնի: Ածխածինը յուրաքանչյուր ջրածնի է վերցնում մեկ բացասական լիցքի համար. Ստացվում է - 3
Չորրորդ կապ քլորի հետ: Ածխածնի եւ քլորի - Ով է ավելի շատ էլեկտրական: Քլոր, դա նշանակում է, որ այս կապակցությամբ էլեկտրոնային զույգը կտեղափոխվի քլորի: Ածխածինը հայտնվում է մեկ դրական լիցքավորում +1:
Այնուհետեւ պարզապես անհրաժեշտ է ծալել. -3 + 1 \u003d -2: Այս ածխածնի օքսիդացման աստիճանը. -2.

Մենք սահմանում ենք յուրաքանչյուր ածխածնի ատոմի օքսիդացման աստիճանը.

Ածխածինը երեք կապ ունի ջրածնի հետ: Ածխածնի եւ ջրածնի - ով է ավելի շատ էլեկտրաէներգիա: Ածխածնի, դա նշանակում է, որ այս երեք պարտատոմսերը էլեկտրոնային զույգը կտեղափոխվի դեպի ածխածնի: Ածխածինը յուրաքանչյուր ջրածնի է վերցնում մեկ բացասական լիցքի համար. Ստացվում է - 3
Եվ մեկ այլ կապ մեկ այլ ածխածնի հետ: Ածխածնի եւ այլ ածխածնի - նրանց էլեկտրականությունն հավասար է, ուստի էլեկտրոնային զույգի տեղաշարժը տեղի չի ունենում (կապը բեւեռ չէ): 

Այս ատոմը երկու կապ ունի մեկ թթվածնի ատոմի հետ, եւ մեկ այլ կապեր մեկ այլ թթվածնի ատոմի հետ (որպես Oh Group- ի մաս): Ավելի շատ էլեկտրաէներգիայի թթվածնի ատոմներ երեք պարտատոմսերով հետաձգում են էլեկտրոնային զույգը ածխածնիից, ածխածինը, +3:
Չորրորդ փողկապը ածխածինը կապված է մեկ այլ ածխածնի հետ, քանի որ մենք արդեն ասել ենք, այս կապակցությամբ էլեկտրոնը չի տեղափոխվում:


Երկու պարտատոմսեր, ածխածինը կապված է ջրածնի ատոմների հետ: Ածխածինը, քանի որ ավելի շատ էլեկտրացանցը ինքն իրեն հետաձգեց մեկ զույգ էլեկտրոնային էլեկտրոնի վրա `ջրածնի հետ յուրաքանչյուր կապի համար, ձեռք է բերում -2:
Ածխածնի կրկնակի ստրկությունը կապված է թթվածնի ատոմի հետ: Լրացուցիչ էլեկտրաէներգիայի թթվածինը խտացնում է մեկ էլեկտրոնային զույգ յուրաքանչյուր կապի համար: Միասին ստացվում է ածխածնի մեջ, երկու էլեկտրոնային զույգ հետաձգվում է: Ածխածինը ձեռք է բերում +2 լիցք:
Միասին ստացվում է +2 -2 \u003d 0:

Մենք սահմանում ենք այս ածխածնի ատոմի օքսիդացման աստիճանը.
Ավելի շատ էլեկտրաէներգիայի ազոտի հետ եռակի փոխհարաբերություններ. Ածխածնի լիցքավորում է +3, ածխածնի կողմնակալության պատճառով ածխածնի պատճառով չի առաջանում:

Օքսիդացման պերմանգանատ:
Ինչ է լինելու Smintaganate- ի հետ:
Redox ռեակցիան Permanganate- ի հետ կարող է հոսել տարբեր լրատվամիջոցներում (չեզոք, ալկալային, թթու): Եվ դա կախված է շրջակա միջավայրից, ինչպես որ կա արձագանքը, եւ ինչ ապրանքներ են ձեւավորվում:
Հետեւաբար, այն կարող է անցնել երեք ուղղություններով.

Վերականգնվում է Permanganate- ը, որը օքսիդացուցիչ լինելը վերականգնվում է: Ահա դրա վերականգնման արտադրանքը.
- Գոլորշի միջին.
Չորեքշաբթի օրը թթվացված է ծծմբաթթուով (H 2 So 4): Մանգանը վերականգնվում է օքսիդացման աստիճանի +2: Եւ վերականգնման արտադրանքը կլինի.
Kmno 4 + h 2 so 4 → mnso 4 + k 2 so 4 + h 2 O
- Ալկալային միջավայր.
Ալկալինի միջավայր ստեղծելու համար ավելացվում է բավականին կենտրոնացված ալկալ (KOH): Մանգանը վերականգնվում է օքսիդացման աստիճանի +6: Վերականգնման արտադրանք
Kmno 4 + koh → k 2 mno 4 + h 2 O
- Չեզոք միջավայր (եւ թույլ ալկալո)).
Չեզոք միջավայրում, բացի Permanganate- ի, ջուրը նաեւ մտնում է ռեակցիա (որը մենք գրում ենք հավասարման ձախ կողմում), մանգան կվերականգնվի +4 (MNO 2),
Kmno 4 + h 2 o → Mno 2 + Koh
Եվ մի փոքր ալկալային միջավայրում (KOH ցածր կոնցենտրացիայի լուծման առկայության դեպքում).
Kmno 4 + Koh → Mno 2 + H 2 O

Ինչ է լինելու օրգանական:
Առաջին բանը, որ դուք պետք է սովորեք, ամեն ինչ սկսվում է ալկոհոլով: Սա օքսիդացման սկզբնական փուլն է: Օքսիդացումը ենթարկվում է այդ ածխածնի, որին կցված է հիդրոքսիլային խումբը:
Օքսիդացման ընթացքում ածխածնի ատոմը «ձեռք է բերում» թթվածնի հետ կապ: Հետեւաբար, երբ գրված է օքսիդացման ռեակցիայի սխեման, [O] գրված է սլաքի վերեւում.
Առաջնային ալկոհոլ Օվկիանոլները առաջին հերթին Ալդեհիդին, ապա `կարբոքսիլային թթու:

Օքսիդացում Երկրորդային ալկոհոլ Դուրս երկրորդ փուլում: Քանի որ ածխածինը հանձնվում է, Կետոնը ձեւավորվում է, եւ ոչ թե Ալդեհիդը (Cetone Group- ում ածխածնի ատոմն արդեն իսկ ի վիճակի չէ կապել հիդրոքսիլ խմբի հետ).

Կետոններ, Երրորդային ալկոհոլներ մի քանազոր carboxylic թթուներ Հաջորդը այլեւս օքսիդացում.

Օքսիդացման գործընթացը քայլ առ քայլ, մինչդեռ կա օքսիդացման եւ դրա համար կա բոլոր պայմանները, արձագանքը գալիս է: Ամեն ինչ ավարտվում է այն արտադրանքով, որը այս պայմաններում չի օքսիդացնում. Երրորդային ալկոհոլ, ketone կամ թթու:
Հարկ է նշել մեթանոլի օքսիդացման փուլը: Բացի այդ, այն օքսիդացվում է համապատասխան Aldehyde- ին, ապա համապատասխան թթվի համար.

Այս ապրանքի առանձնահատկությունն է (ձեւավորաթթու), որ Carboxyl խմբի ածխածինը կապված է ջրածնի հետ, եւ եթե ուշադիր նայեք, կարող եք տեսնել, որ Ալդեհիդի խումբը ոչինչ չէ:

Եվ Ալդեհիդային խումբը, ինչպես արդեն պարզեցինք, օքսիդացվում է Carboxyl- ին.

Ճանաչել է արդյունքում ստացված նյութը: Դրա համախառն բանաձեւ H 2 CO 3: Սա կոալիցի թթու է, որը բաժանվում է ածխաթթու գազից եւ ջրից.
H 2 CO 3 → H 2 O + CO 2
Հետեւաբար, մեթանոլը, մրջյուն ալդեհիդը եւ ձեւավորաթթունը (Ալդեհիդի խմբի հաշվին) օքսիդացվում են ածխաթթու գազի վրա:
Փափուկ օքսիդացում:
Փափուկ օքսիդացումն է Առանց ուժեղ ջեռուցման չեզոք կամ թեթեւակի միջին ջեռուցման (արձագանքման ընթացքում գրված է 0) ° կամ 20: °) .
Կարեւոր է հիշել, որ ալկոհոլները մեղմ պայմաններում օքսիդացվում են: Հետեւաբար, եթե դրանք ձեւավորվեն, ապա օքսիդացում եւ դադարում են: Ինչ նյութեր կմիանան փափուկ օքսիդացման արձագանքին:
- Պարունակող կրկնակի պարտատոմս C \u003d C (Wagner Reaction):
Միեւնույն ժամանակ, π-Bond- ը կոտրված է, եւ ազատագրված պարտատոմսերը «նստում են» հիդրոքսիլային խմբի վրա: Ստացվում է կրկնակի ալկոհոլ.

Մենք գրում ենք էթիլենային (էթված) փափուկ օքսիդացման արձագանքը: Մենք գրում ենք մեկնարկային նյութերը եւ կանխատեսում արտադրանքը: Միեւնույն ժամանակ, H 2 O- ն եւ COH- ն դեռ չեն գրում. Կարող են պարզվել, որ երկուսն էլ հավասարման եւ ձախ կողմում են: Եւ անմիջապես որոշեք մասնակից նյութերի օքսիդացման աստիճանը.

Մենք կկատարենք էլեկտրոնային հավասարակշռություն (մենք նկատի ունենք, որ նվազեցման գործակալը երկու - երկու ածխածնի ատոմ է, դրանք օքսիդացվում են առանձին).

Ընտրեք գործակիցները.

Ի վերջո, անհրաժեշտ է ավելացնել անհայտ կորած արտադրանքներ (H 2 O եւ Koh): The իշտը Կալիումի պակասը. Դա նշանակում է, որ Ալկալին ճիշտ կլինի: Մենք գործակիցը դնում ենք դրա դիմաց: Ձախ կողմում չկա բավարարված ջրածին, դա նշանակում է, որ ջուրը մնացել է: Մենք դրա դիմաց գործակիցը դնում ենք.

Մենք նույնն ենք անում պրոպիլենով (պրոպան).


Հաճախ տեղավորվում են ցիկլոկան: Թող նա ձեզ չի ամաչում: Սա սովորական ածխաջրածին է `կրկնակի կապով.

Ուր էլ լինի այս երկակի կապը, օքսիդացումը հավասարապես կընթանա.

- Պարունակում է Aldehyde Group.
Aldehyde Group- ը ավելի ռեակտիվ է (ավելի հեշտ է արձագանքել), քան ալկոհոլը: Հետեւաբար, ալդեհիդը օքսիդացվի: Թթու:

Մտածեք acetaldehyde (էթանեւ) օրինակով: Մենք ռեակտիվներ եւ ապրանքներ ենք գրում եւ դնում օքսիդացման աստիճանը: Մենք կկատարենք հավասարակշռություն եւ գործակիցները դնում ենք նվազեցման գործակալից եւ օքսիդացնող գործակալից:

Չեզոք միջավայրում եւ արձագանքման մի փոքր ալկալային ընթացքը փոքր-ինչ այլ կլինի:
Չեզոք միջավայրում, ինչպես մենք հիշում ենք, հավասարման ձախ կողմում մենք ջուր ենք գրում, եւ Ալկալիի հավասարման ճիշտ մասում (ձեւավորվել է արձագանքի ընթացքում).

Այս դեպքում թթուն եւ ալկալիները հայտնաբերվում են մեկ խառնուրդում: Չեզոքացումը տեղի է ունենում:

Դրանք չեն կարող գոյություն ունենալ մոտ եւ արձագանքել, աղի ձեւեր.
Միեւնույն ժամանակ, եթե մենք նայենք գործակիցներին հավասարման մեջ, մենք կհասկանանք, որ թթուները 3 աղոթում են, եւ Ալկալի 2 աղոթում է: 2 Աղոթելով Ալկալին կարող է չեզոքացնել ընդամենը 2 աղոթող թթուներ (ձեւավորվում է 2 աղոթքի աղ): Եւ մնում է թթու մեկ ցիտ: Հետեւաբար, վերջնական հավասարումը այսպիսին կլինի.

Մի փոքր ալկալային միջավայրում այն \u200b\u200bալկալին է ավելցուկով. Այն ավելացվում է արձագանքին, այնպես որ բոլոր թթունը չեզոքացված է.

Նմանատիպ իրավիճակ է առաջանում, երբ մեթանալը օքսիդացվում է: Նա, ինչպես հիշում ենք, օքսիդացվում է ածխաթթու գազի.

Այն պետք է հիշել, որ ածխածնի օքսիդի (IV) CO 2- ը թթվային է: Եւ կարձագանքի Ալկալիի հետ: Եվ քանի որ ածուխ թթունը երկկողմանի է, կարելի է ձեւավորել ինչպես թթու աղ, եւ միջին: Դա կախված է Ալկալի եւ ածխածնի երկօքսիդի միջեւ հարաբերակցությունից.
Եթե \u200b\u200bԱլկալը վերաբերում է ածխաթթու գազին, 2: 1, ապա կլինի միջին աղ:
Կամ ալկալիները կարող են զգալիորեն ավելին լինել (ավելի քան երկու անգամ): Եթե \u200b\u200bդա ավելի քան երկու անգամ է, ապա ալկալիսի մնացորդը կմնա.
3koh + Co 2 → K 2 CO 3 + H 2 O + KOH
Դա տեղի կունենա ալկալային միջավայրում (որտեղ Ալկալի ավելցուկը, քանի որ այն ավելացվում է ռեակցիայի ռեակցիայի խառնուրդին) կամ չեզոք միջավայրում, երբ Ալկալին շատ բան է ձեւավորվում:
Բայց եթե Ալկալը վերաբերում է ածխաթթու գազին, 1: 1, դա կլինի թթվային աղ.
Koh + Co 2 → Khco 3
Եթե \u200b\u200bածխածնի երկօքսիդը ձեզանից ավելի մեծ է, այն մնում է ավելորդ.
Koh + 2Co 2 → Khco 3 + Co 2
Սա կլինի չեզոք միջավայրում, եթե Ալկալին ձեւավորվի ոչ բավարար:
Մենք գրում ենք աղբյուրի նյութեր, ապրանքներ, մենք կհամալսվենք օքսիդացման հավասարակշռությունը օքսիդացնող միջոցի դիմաց, նվազեցնելով գործակալը եւ դրանցից ձեւավորված արտադրանքները.

Չեզոք միջավայրում աջ կողմում կստեղծվի Ալկալի (4 կմ).

Այժմ անհրաժեշտ է հասկանալ, թե ինչն է ձեւավորվելու CO 2 եւ չորս ալկալային խլուրդի փոխազդեցությամբ:
3Co 2 + 4KOH → 3khco 3 + koh
Khco 3 + Koh → K 2 Co 3 + H 2 O
Հետեւաբար, պարզվում է, որ այսպիսին է.
3Co 2 + 4KOH → 2khco 3 + k 2 CO 3 + H 2 O
Հետեւաբար, հավասարումների ճիշտ մասում մենք գրում ենք երկու աղոթքային ակոս եւ կարբոնատ մեկ մոլ:

Եվ թույլ ալկալային միջավայրում նման խնդիրներ չկան. Այն պատճառով, որ Ալկալի ավելցուկը կստեղծվի միջին աղով.

Նույնը կլինի օքսիդաթթվի ալդեհիդի օքսիդացման ժամանակ.

Ինչպես նախորդ օրինակով, ձեւավորվում է դիբասե թթու, իսկ 4 աղոթող Ալկալին պետք է լինեն հավասարման վրա (որպես 4 աղոթող permanganate):
Չեզոք միջավայրում, կրկին, ամբողջ ալկալին բավարար չէ ամբողջ թթվի ամբողջական չեզոքացման համար:
Երեք աղոթող Ալկալիսը գնում է թթվային աղի ձեւավորմամբ, մնում է Ալկալիի մեկ մոլը.
3 Hooc-Cooh + 4KOH → 3kooc-Cooh + Koh
Եվ այս մեկ մոլեխալը մտնում է մեկ թթու աղի հետ փոխազդեցության մեջ.
Kooc-Cooh + Koh → Kooc-Cook + H 2 O
Ստացվում է, որ այսպես է.
3 Hooc-Cooh + 4Koh → 2kooc-Cooh + KOOC-Cook + H 2 O
Վերջի հավասարումը.

Թույլ ալկալային միջավայրում միջին աղը ձեւավորվում է ալկալիների ավելցուկի պատճառով.

- Պարունակում է եռակի փոխհարաբերություններԳ.≡ Գ..
Հիշեք, թե ինչն էր կրկնակի կապի հետ կապերի փափուկ օքսիդացման հետ: Եթե \u200b\u200bչեք հիշում, ապա ոլորեք ետ - Հիշեք:
Պարտատոմսը փխրուն է, ածխածնի ատոմները կցվում են հիդրոքսիլ խմբի երկայնքով: Ահա նույն սկզբունքը: Հիանալի է միայն հիշել, որ եռակի կապի մեջ կա երկու π պարտատոմսեր: Սկզբում դա տեղի է ունենում առաջին π- կապի վրա.
Այնուհետեւ մեկ այլ π-հաղորդակցության վրա.

Այն կառուցվածքը, որում կա ածխածնի ատոմ, ունի երկու հիդրոքսիլ խմբեր, ծայրաստիճան անկայուն: Երբ քիմիայի մեջ ինչ-որ բան չի պահպանվում, այն ձգտում է «ընկնել»: Water ուրը ընկնում է, ինչպես այսպիսին է.

Ստացվում է Carbonyl Group- ը:
Դիտարկենք օրինակներ.
Էթին (ացետիլեն): Դիտարկենք այս նյութի օքսիդացման փուլերը.

Cleaner րի մաքրող.




Ինչպես նախորդ օրինակով, թթվային եւ ալկալային մեկ ռեակցիայի խառնուրդով: Չեզոքացումը տեղի է ունենում. Աղի ձեւեր: Ինչպես երեւում է Permanganate- ի առաջ գործակիցը, Ալկալին կլինի 8 խալ, այսինքն, դա բավարար է թթու չեզոքացման համար: Վերջի հավասարումը.

Հաշվի առեք Boudin-2 օքսիդացումը.

Cleaner րի մաքրող.

Այստեղ թթունը չի ձեւավորվում, ուստի անհրաժեշտ չէ հիմարացնել չեզոքացման պատճառով:
Արձագանքի հավասարումը.

Այս տարբերությունները (ածխածնի օքսիդացման եզրին եւ շղթայի կեսին) պայծառորեն դրսեւորվում են Պենտինայի օրինակով.

Cleaner րի մաքրող.

Պարզվում է հետաքրքիր կառուցվածքի մի նյութ.

Aldehyde Group- ը շարունակում է օքսիդացնել.
Մենք գրում ենք մեկնարկային նյութերը, ապրանքները, որոնք որոշում են օքսիդացման աստիճանը, մենք կլինենք հավասարակշռված, պարզ գործակիցներ նախքան օքսիդացնող գործակալը եւ գործակալը.

Ալկալին պետք է ձեւավորի 2 կույտ (քանի որ Permanganate 2-ից առաջ գործակիցը), հետեւաբար, ամբողջ թթուն չեզոքացվում է.

Կոշտ օքսիդացում.
Քրտնաջան օքսիդացումը օքսիդացում է թթու, Վերացնել Միջին: Ինչպես նաեւ չեզոք (կամ ցածր ալկալային), բայց երբ ջեռուցվում է.
Թթվային միջավայրում նույնպես ջեռուցվում է: Բայց այդ ծանր օքսիդացումը չի անցնում թթվային միջավայրում, ջեռուցումը նախապայման է:
Ինչ նյութեր են ենթարկվելու ծանր օքսիդացման: (Սկզբում մենք վերլուծելու ենք միայն թթվային միջավայրում, այնուհետեւ ավելացնել նրբություններ, որոնք առաջանում են ուժեղ ալկոհոլային եւ չեզոք կամ թույլ ալկալային օքսիդացումով):
Քրտնաջան օքսիդացումով գործընթացը անցնում է առավելագույնը: Չնայած կա, որ օքսիդացված է. Օքսիդացումը գնում է:
- Ալկոհոլներ: Ալդեհիդներ.
Հաշվի առեք էթանոլի օքսիդացումը: Այն օքսիդացվում է թթվին.

Գրառման հավասարումը: Մենք գրում ենք մեկնարկային նյութերը, OSR- ի արտադրանքները, դնում են օքսիդացման աստիճանը, կազմում են հավասարակշռությունը: Կարգավորեք արձագանքը.

Եթե \u200b\u200bարձագանքն իրականացվում է Ալդեհիդեի եռացրած կետում, երբ այն ձեւավորվի, այն գոլորշիանում է (թռչելու է) ռեակցիայի խառնուրդից, ոչ այնքան, քան օքսիդացմանը: Նույն ազդեցությունը կարելի է հասնել շատ մեղմ պայմաններում (թույլ ջեռուցում): Այս դեպքում մենք Aldehyde- ն ենք գրում որպես արտադրանք.

Հաշվի առեք երկրորդային ալկոհոլի օքսիդացումը Propanol-2- ի օրինակով: Ինչպես արդեն նշվեց, երկրորդ փուլում օքսիդացումը կոտրվում է (կարբոնլ բաղադրության ձեւավորումը): Քանի որ Ketone- ն ձեւավորվում է, որը օքսիդացված չէ: Արձագանքի հավասարումը.

Ալդեհիդների օքսիդացումը դիտարկվում է էթելի թեմայով: Այն նաեւ օքսիդացվում է թթվին.

Արձագանքի հավասարումը.

Methanal- ը եւ Methanol- ը, ինչպես նշվեց ավելի վաղ, օքսիդացված ածխաթթու երկօքսիդին.

Մեթանալ.

- Բազմաթիվ պարտատոմսեր պարունակող.
Այս դեպքում շղթան փչում է բազմաթիվ հաղորդակցության մեջ: Եւ այն ձեւավորված ատոմները օքսիդացված են (ձեռք բերեք կապ `թթվածնի հետ): Օվկերուկները որքան հնարավոր է:
Երբ խզվում են գրություններից կրկնակի կապը, ձեւավորվում են կարբոնլի միացություններ (ներքեւում գտնվող դիագրամում. Մեկ պայթյունից `Ալդեհիդից)

![]()
Մենք կվերլուծենք Պենտեն -2-ի օքսիդացումը.

«Գրություններ» օքսիդացում.

Ստացվում է, որ ձեւավորվում է երկու թթուն: Մենք գրում ենք մեկնարկային նյութերն ու արտադրանքները: Մենք սահմանում ենք ատոմներում օքսիդացման աստիճաններ, որոնք այն փոխում են, հավասարակշռված են, հավասարեցնում են արձագանքը. 
Էլեկտրոնային մնացորդը կազմելով, մենք նկատի ունենք, որ նվազեցնող գործակալը երկու - երկու ածխածնի ատոմ է, դրանք առանձին օքսիդացվում են.

Թթուը միշտ չէ, որ ձեւավորվի: Մենք վերլուծելու ենք, օրինակ, 2-մեթիլբուտենի օքսիդացում.

Արձագանքի հավասարումը.

Բացարձակապես նույն սկզբունքը, երբ եռակի կապով օքսիդացնող միացությունները (միայն օքսիդացումը միացված է թթվի ձեւավորմամբ, առանց Ալդեհիդի միջանկյալ ձեւավորման).

Արձագանքի հավասարումը.

Երբ բազմակի կապը գտնվում է հենց մեջտեղում, ապա ոչ երկու ապրանքատեսակ, այլեւ մեկը: Քանի որ «գրությունները» նույնն են, եւ դրանք օքսիդացվում են նույն ապրանքների վրա.

Արձագանքի հավասարումը.

- Երկու անգամ թագի թթու.
Մի թթու կա, որ կարբոքսիլային խմբերը (պսակներ) միացված են միմյանց.
Սա կախարդական թթու է: Երկու պսակները դժվար է համախմբվել: Դա, անշուշտ, կայուն է նորմալ պայմաններում: Բայց այն պատճառով, որ դրա մեջ երկու կարբոքսիլային խմբեր կապված են միմյանց հետ, այն պակաս կայուն է, քան այլ carboxylic թթուները:
Եվ, հետեւաբար, հատկապես կոշտ միջավայրերով, այն կարող է օքսիդացվել: «Երկու պսակների» միջեւ ընդմիջում կա.

Արձագանքի հավասարումը.

- Բենզոլի (եւ դրանց ածանցյալների) գոմոլոգները.
Բենզոլն ինքնին օքսիդացված չէ, այն պատճառով, որ բույրերը այս կառուցվածքը շատ կայուն են դարձնում 
Բայց նրա հոմոլոգիան օքսիդացվում է: Միեւնույն ժամանակ, շղթայի ընդմիջումները, գլխավորը `իմանալ, թե որտեղ է: Կան որոշ սկզբունքներ.
- Բենզոլի օղակը ինքնին չի ոչնչացնում եւ մնում է մինչեւ վերջ, հաղորդակցության փչացումը տեղի է ունենում արմատականության մեջ:
- Օքսիսում է ատոմ, որն ուղղակիորեն կապված է բենզոլի օղակի հետ: Եթե \u200b\u200bդրանից հետո արմատականորեն ածխածնի շղթան շարունակվի, ապա դրանից հետո բացը կլինի:


Մենք վերլուծելու ենք մեթիլ բենզինի օքսիդացումը: Արմատական \u200b\u200bօքսիդացնում է մեկ ածխածնի ատոմ. 
Արձագանքի հավասարումը.

Մենք կվերլուծենք Իզոբուտիլբենզենի օքսիդացումը.

Արձագանքի հավասարումը.

Մենք կվերլուծենք երկրորդ-բուտիլբենզենի օքսիդացումը.

Արձագանքի հավասարումը.

Մի քանի արմատականներով բենզոլի (եւ ածանցյալների ածանցյալներ) օքսիդացման օքսիդացումներում ձեւավորվում են երկու-երեք եւ ավելի մեծ անուշաբույր թթուներ: Օրինակ, 1,2-դիմեթիլբենզի օքսիդացում.

Բենզոլի հոմոլոգիաների ածանցյալները (որով բենզոլային օղակը ածխաջրածինային արմատականներ չէ), օքսիդացրեք նույնը: Մեկ այլ ֆունկցիոնալ խումբ չի խանգարում բենզոլի օղակին.


Ենթաօրենսդրական Ալգորիթմ «Ինչպես արձանագրել թթվային միջավայրում ծանր օքսիդացման պերմանգանատի պատասխանը».
- Գրանցեք մեկնարկային նյութեր (օրգանական + KMNO 4 + H 2 SO 4):
- Գրեք օրգանական օքսիդացման արտադրանքներ (ալկոհոլային խմբեր, բազմաթիվ պարտատոմսեր, ինչպես նաեւ բենզոլային հոմոլոգներ պարունակող միացություններ):
- Գրեք permanganate վերականգնման արտադրանքը (MNSO 4 + K 2 So 4 + H 2 O):
- Որոշեք OSR- ի մասնակիցներից օքսիդացման աստիճաններ: Հավասարակշռություն: Սայթաքել օքսիդացնող միջոցի գործակիցը եւ նվազեցնող գործակալը, ինչպես նաեւ դրանցից ձեւավորված նյութերը:
- Այնուհետեւ առաջարկվում է հաշվարկել, թե քանի սուլֆատ անիոն է հավասարման ճիշտ մասում, այսին համաձայն, ձախ կողմում գտնվող ծծմբաթթվի դիմաց գործակիցը դրեք:
- Վերջում գործակիցը դրեց ջրի առաջ:
Ծանր օքսիդացում ուժեղ այլընտրանքային միջին եւ չեզոք կամ թույլ ալկալային (երբ ջեռուցվում է).
Այս ռեակցիաները շատ ավելի տարածված են: Կարելի է ասել, որ նման արձագանքները էկզոտիկ են: Եվ ինչպես դա պետք է արվի ցանկացած էկզոտիկ ռեակցիաներով, սրանք առավել հակասական էին:
Կոշտ օքսիդացում Այն կոշտ է Աֆրիկայում, ուստի օրգանական օքսիդացվում է այնպես, ինչպես թթվային միջավայրում:
Առանձին-առանձին, մենք չենք ապամոնտաժելու արձագանքը յուրաքանչյուր դասի համար, քանի որ ընդհանուր սկզբունքն արդեն նախանշված է: Մենք վերլուծելու ենք միայն նրբությունները:
Վերացրեք միջավայրը :
Խստորեն ջրիմուռներում պերմանգանատը վերականգնվում է օքսիդացման աստիճանի +6 (Կալիումի կառավարիչ).
KMNO 4 + KOH → K 2 MNO 4.
Ուժեղ ալկալի Ալկալիում միշտ կա ավելցուկ, ուստի կանցկացվի ամբողջական չեզոքացում. Եթե ածխաթթու գազը ձեւավորվի.
Օրինակ, ֆրոֆենի օքսիդացումը.

Էթիլբենզեն օքսիդացում.

Պիտակի կամ չեզոք միջոց, երբ ջեռուցվում է :
Այն նաեւ պետք է միշտ հաշվի առնել չեզոքացման հնարավորությունը:
Եթե \u200b\u200bձեւավորվում է չեզոք միջավայրում եւ թթվային կամ ածխաթթու երկօքսիդի (թթվի կամ ածխաթթու երկօքսիդ) օքսիդացման հոսքեր, ապա արդյունքում ստացված ալկոհոլը կեզոքացնի այս թթու բաղադրիչը: Բայց միշտ չէ, որ Ալկալին բավարար է թթու լիարժեք չեզոքացման համար:
Երբ ալդեհիդները օքսիդացվում են, օրինակ, դա բավարար չէ (օքսիդացումը կընթանա նույն ձեւով, ինչպես մեղմ պայմաններում), ջերմաստիճանը պարզապես արագացնում է արձագանքը): Հետեւաբար, ձեւավորվում է աղ եւ թթու (կոպիտ խոսելու համար):
Մենք քննարկեցինք այն, երբ նրանք ապամոնտաժում են Ալդեհիդների փափուկ օքսիդացումը:
Հետեւաբար, եթե թթվը ձեւավորվի չեզոք միջավայրում, դուք պետք է ուշադիր նայեք, արդյոք դա բավարար է ամբողջ թթվի չեզոքացման համար: Հատուկ ուշադրություն պետք է դարձնել պոլիպիկ թթուների չեզոքացմանը:
Մի փոքր ալկալային միջավայրում միայն միջին աղերը ձեւավորվում են ալկալիների բավարար քանակի պատճառով, որպես ալկալիների ավելցուկ:
Որպես կանոն, չեզոք միջավայրում օքսիդացման ժամանակ Ալկալը բավարար է: Եվ արձագանքման հավասարումը, որը չեզոք է, որ թույլ ալկալային միջավայրում նույնը կլինի:
Օրինակ, մենք կվերլուծենք էթիլբենզենի օքսիդացումը.


Ալկալին բավարար է թթվային միացությունների ամբողջական չեզոքացման համար, նույնիսկ ավելցուկը մնում է.

3 Աղոթքի ալկալին սպառվում է `1 մնում է:
Վերջի հավասարումը.

Չեզոք եւ ցածր ալկալային միջավայրում այս արձագանքը կընթանա հավասարապես (ցածր ալկալային միջավայրում չկա ալկալիներ, բայց դա չի նշանակում, որ դա պարզապես չի մտնում արձագանքը):
Կալիումի երկարակյաց (բարքոմատ) ներգրավված ռեալոքս ռեակցիաներ:
Քննությունում Bichromat- ը չունի օրգանական օքսիդացման նման լայն տեսականի:
Բարքոմատի կողմից օքսիդացումը սովորաբար իրականացվում է միայն թթվային միջավայրում: Այս քրոմը վերականգնվում է +3: Վերականգնման արտադրանք.
Օքսիդացումը կլինի կոշտ: Արձագանքը շատ նման կլինի permanganate- ի օքսիդացմանը: Նույն նյութերը կօգտագործվեն, որ դրանք օքսիդավորված են թթվային միջավայրում գտնվող permanganate- ով, կձեւավորվի նույն արտադրանքը:
Մենք կվերլուծենք որոշ արձագանքներ:
Հաշվի առեք ալկոհոլի օքսիդացումը: Եթե \u200b\u200bմենք օքսիդացում ենք իրականացնում Ալդեհիդի եռացող կետում, ապա դա կհեռանա նրանց արձագանքման խառնուրդը, առանց ենթարկվելու օքսիդացման.

Հակառակ դեպքում ալկոհոլը կարող է ուղղակիորեն օքսիդացվել թթու:
Նախորդ ռեակցիայի ընթացքում ստացված ալդեհիդը կարող է «բռնել» եւ այն օքսիդացված թթու է դարձնում.

Cyclohexanol- ի օքսիդացում: Cyclohexanol- ը երկրորդական ալկոհոլ է, ուստի ձեւավորվում է ketone- ը.

Եթե \u200b\u200bդժվար է որոշել նման բանաձեւով ածխածնի ատոմների օքսիդացման աստիճանը, ապա հնարավոր է նկարել նախագծի վրա.

Արձագանքի հավասարումը.

Դիտարկենք ցիկլոպենտենի օքսիդացումը:
Կրկնակի կապը կոտրվում է (ցիկլը բացվում է), այն ատոմները, որոնք այն կազմում են առավելագույնը (այս դեպքում, Carboxyl խմբում):


Քննության օքսիդացման որոշ առանձնահատկություններ, որոնց հետ մենք այնքան էլ համաձայն չենք:
Այս «կանոնները», սկզբունքներն ու արձագանքները, որոնք կքննարկվեն այս բաժնում, մենք բոլորովին ճիշտ չենք համարում: Նրանք հակասում են ոչ միայն իրական իրավիճակի (քիմիայի որպես գիտություն), այլեւ մասնավորապես դպրոցական ծրագրի եւ քննության ներքին տրամաբանությունը:
Բայց, այնուամենայնիվ, մենք ստիպված ենք այս նյութը ճշգրիտ տալ այն ձեւով, որը պահանջում է քննությունը:
Դա կլինի ծանր օքսիդացման մասին:
Հիշեք, թե ինչպես են գոմոլոգները օքսիդացվում եւ նրանց արտասանված ծանր պայմաններում: Արմատականները ամբողջովին կոտրված են. Ձեւավորվում են Carboxyl խմբերը: Գրությունները ենթարկվում են օքսիդացման արդեն «ինքնուրույն».

Այսպիսով, եթե հիդրոքսիլային խումբը հանկարծ արմատական \u200b\u200bէ կամ բազմաթիվ հաղորդակցություն, պետք է մոռանալ, որ բենզինի մատանին կա: Արձագանքը կգնա միայն այս ֆունկցիոնալ խմբի վրա (կամ բազմաթիվ հաղորդակցություն):
Ֆունկցիոնալ խումբը եւ բազմաթիվ հաղորդակցման Գոստերը, քան բենզոլային օղակը:

Մենք կվերլուծենք յուրաքանչյուր նյութի օքսիդացում.
Առաջին նյութ.

Դուք չպետք է ուշադրություն դարձնեք այն փաստին, որ կա բենզոլի մատանին: Օգտագործման տեսանկյունից պարզապես երկրորդային ալկոհոլ է: Երկրորդային ալկոհոլները օքսիդացվում են Քեթոնների համար, իսկ Քեթոնները օքսիդացված չեն.

Թող այս նյութը օքսիդացվի BichRomate- ի կողմից.

Երկրորդ նյութ.

Այս նյութը օքսիդացվում է, պարզապես որպես երկակի կապակցված կապ (մենք ուշադրություն չենք դարձնում բենզինի մատանին).

Թող այն օքսիդացվի չեզոք պերմանգանատի մեջ, երբ ջեռուցվում է.

Ձեւավորեց Ալկալի, ածխաթթու գազի ամբողջական չեզոքացման համար.
2koh + Co 2 → K 2 CO 3 + H 2 O
Ընդհանուր հավասարումը.

Երրորդ նյութի օքսիդացում.

Ենթադրենք, որ օքսիդացումը կալիումի թափանցում կլինի թթվային միջավայրում.

Չորրորդ նյութի օքսիդացում.

Այն օքսիդացվում է ուժեղացուցիչի միջավայրում: Արձագանքման հավասարումը կլինի.

Վերջապես, այն այնքան օքսիդացված է վինիլբենզենից.

Եվ այն օքսիդացվում է բենզոաթթվի համար, անհրաժեշտ է հիշել, որ քննության տրամաբանության համաձայն, այն այնքան օքսիդացված է, քանի որ այն բենզինի ածանցյալ է: Եվ քանի որ այն պարունակում է կրկնակի կապ:
Եզրակացություն.
Ամեն ինչ այն է, ինչ դուք պետք է իմանաք ռեդոքսային ռեակցիաների մասին, որոնք ներգրավված են օրգանական լեզվով permanganate եւ bichromate:
Մի զարմացեք, եթե այս հոդվածում որոշ պահեր են սահմանված, առաջին անգամ եք լսում: Ինչպես արդեն նշվեց, այս թեման շատ ընդարձակ եւ հակասական է: Եվ չնայած դրան, ինչ-ինչ պատճառներով նա չափազանց փոքր ուշադրություն է դարձնում:
Ինչպես կարող եք համոզվել, երկու-երեք ռեակցիաները չեն բացատրում այս ռեակցիաների բոլոր նախշերը: Այստեղ ձեզ հարկավոր է ինտեգրված մոտեցում եւ բոլոր պահերի մանրամասն բացատրություն: Դժբախտաբար, դասագրքերում եւ ինտերնետային ռեսուրսներում թեման ամբողջությամբ բացահայտված չէ, թե ընդհանրապես չի բացահայտվում:
Փորձեցի վերացնել այս թերությունները եւ թերությունները եւ ամբողջությամբ դիտարկել այս թեման, եւ ոչ թե մասամբ: Հուսով եմ, որ ղեկավարել եմ այն:
Շնորհակալ եմ ձեր ուշադրության համար, բոլորդ լավն եք: Քիմիական գիտության եւ քննությունների անցկացման հաջողություններ:
4.5. Ալկենեսի օքսիդացում
Ալկենի օքսիդացման ռեակցիաները խորհուրդ են տրվում բաժանվել երկու մեծ խմբերի. Արձագանքներ, որոնցում պահպանվում է ածխածնի կմախքը եւ կրկնակի պարտատոմսերի մոլեկուլի ածխածնի կմախքի օքսիդատիվ ոչնչացման արձագանքը: Արձագանքների առաջին խումբը ներառում է էպոքսացում, ինչպես նաեւ հիդրօքսիդավորում, որի արդյունքում առաջանում է Վերեւում գտնվող դիոլների (գլիկոլ) ձեւավորումը: Հիդրոքսիլացիայի ընթացքում ցիկլային Ալկենեսի դեպքում ձեւավորվում է տրանս- կամ ԱՊՀ-Կարողներ: Մեկ այլ խումբ ներառում է օզոնոլիզ եւ Ալկենեսի սպառիչ օքսիդացման արձագանք, ինչը հանգեցնում է տարբեր տեսակի կարբոնիկ միացությունների եւ կարբինգիկ \u200b\u200bթթուների ձեւավորմանը:
4.5.A. Alkenes- ի օքսիդացման ռեակցիաները `ածխածնի կմախքը պահպանելիս
1. Epoxidation (արձագանք N.A. Prilezhev, 1909 գ)
Aciclic- ի եւ ցիկլային ալկեները շփվելիս (suprachlotes) RCOOOH- ի հետ շփվելիս ոչ բեւեռային, անտարբեր միջին ձեւի էպոքսինգի (Oxirans), այնպես որ արձագանքը կոչվում է էպոքսիդացման ռեակցիա:
Ըստ ժամանակակից նոմենկլատուրայի Jupak - Երկու հոգուց բաղկացած ցիկլը մեկ թթվածնի ատոմով կոչվում է Օքսիրա:
Ալկենեսի էպօքսիդացումը պետք է համարվի որպես սինխրոն, համակարգված գործընթաց, որի միջոցով հիդրոքսիլային կատվի տեսակը ներգրավված չէ իոնիկ միջնորդները: Այլ կերպ ասած, Ալկենեսի էպոքսիդացումը գործընթաց է կար- Troubleto One Onygen Atom- ը կրկնակի պարտատոմսով փոխարինող կազմաձեւի ամբողջական պահպանմամբ երկակի հաղորդակցության համար:
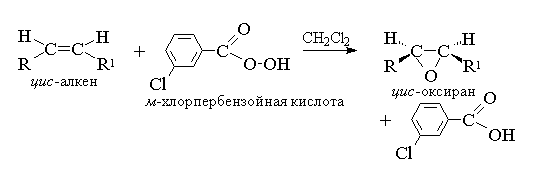

Epoxidation- ի համար առաջարկվել է մեխանիզմ համաձայնեցված գործընթացների:

T. K. Թթվածնի թթվածնի երկկողմանի հարձակման ատոմը հավասարապես հավասար է կրկնակի պարտատոմսերի ինքնաթիռի երկու կողմերին, ձեւավորված օքիրանները կամ Մեսո- Ձեւաթղթեր կամ էնդենոմերների խառնուրդներ: Հետեւյալ պեկուլյոներն օգտագործվում են որպես էպոքսիդացնող նյութեր `Pebenzoic, Տղամարդ-Հլորբենբենզոիկ, մոնոֆերֆթալ, Պերուսում, տրիֆլյուզուս եւ մշտական: Անուշաբույր շարքի perkislotes- ը օգտագործվում է առանձին ռեակտիվների տեսքով, իսկ Perkislotes- ը Aliphatic Rows - CH 3 CO 3 H- ն եւ NSO 3 N- ը մեկուսացված չեն անհատապես, բայց օգտագործվում է փոխգործակցության ընթացքում դրանց ձեւավորումից հետո 30% կամ 90% ջրածնի պերօքսիդի եւ համապատասխան կարբոքսաթթու: Perbenzoic I. Տղամարդ-Հլորբենզուաթթուը \u200b\u200bձեռք է բերվում օքսիդացման միջոցով, համապատասխանաբար, բենզոիկ եւ Տղամարդ-Հլորբենզուաթթուներ `70% ջրածնի պերօքսիդի մետաղական թթվային լուծույթով կամ այս թթուների եւ ջրածնի պերօքսիդի քլորիդի հիդրիդերից:


Monoperfthalic թթու ստացվում է նմանատիպ մեթոդով ֆթալական անհիդրիդ եւ 30% ջրածնի պերօքսիդ:

Սկզբնապես օքսիան ձեռք բերելու համար օգտագործվել են Pebenzoic կամ մոնոպերային թթուներ.

Ներկայումս Epoxidation- ի համար առավել հաճախ օգտագործվում են Տղամարդ-Հլորբենզուաթթու թթու: Ի տարբերություն այլ perkslot- ի, այն կայուն է, երբ երկար ժամանակ պահվում է (մինչեւ 1 տարի) եւ բացարձակապես անվտանգ է կապվելիս: Oxyrants ձեռք են բերվել Acyclic եւ Cyclic Alkenes- ի օքսիդացման ժամանակ Տղամարդ- Mherperbenzoic թթու մեթիլեն քլորիդ լուծույթում, քլորոֆորմ կամ դիօքսան, սովորաբար բավականին բարձր:



Perkislotes- ը հաճախ առաջանում է ուղղակիորեն 90% ջրածնի պերօքսիդի եւ կարբինգիկ \u200b\u200bթթուի արձագանքման խառնուրդում մեթիլեն քլորիդում:


Կրկնակի Bond Alkenes- ը, որը կապված է կարբոնիայի խմբի կամ մեկ այլ ընդունելի փոխարինողի հետ, ցածր ակտիվ եւ դրանց օքսիդացման համար, ավելի լավ է օգտագործել ավելի ուժեղ օքսիդիչներ, ինչպիսիք են TrifluoroCetic թթու անհիդրինից, եւ 90% ջրածնի պերօքսիդը մեթիլեն քլորիդում: Ամենապարզ Oxiran - Etylene օքսիդը ձեռք է բերվում արդյունաբերության մեջ թթվածնի միջոցով թթվածնի օքսիդացումով, որպես արծաթի ներկայությամբ:

2. հակա-Հիդրոքսիլացիա
Օքսիրանի երեք հոգուց բաղկացած օղակը հեշտությամբ բացահայտվում է նուկլեոֆիլային ռեակտիվների լայն տեսականիով: Այս ռեակցիաները մանրամասն կքննարկվեն այն հատվածում, որը նվիրված է acclical եւ ցիկլային պարզ եթեր: Այստեղ կքննարկվի միայն Օքսիրանի հիդրոլիզը: Օքսիրանի հիդրոլիզացումը կատալիզացվում է ինչպես թթուների, այնպես էլ հիմքերի կողմից: Երկու դեպքում էլ ձեւավորվում են վերեւում գտնվող դիոդներ, ես: Glycols: Առաջին փուլում թթու կատալիզատորով թթվածնի թթվածնի ատոմը նախապատվացվում է ցիկլային օքսիայի կատվի ձեւավորմանը, որը բացահայտվում է ջրի մոլեկուլի նուկլեոֆիլային հարձակման հետեւանքով.

Օձի արագությունը լուծելու հիմնական փուլը, որը որոշում է ամբողջ գործընթացի արագությունը, Oxiran- ի պրոտոնացված ձեւով ջրով նուկլեոֆիլային հարձակումը: Մեխանիզմի տեսանկյունից այս գործընթացը նման է բրոմոնում իոնի բացահայտմանը `բրոմիդային իոնի կամ մեկ այլ նուկլեոֆիլ գործակալների միջուկային հարձակմամբ: Այս դիրքերից ստերեոքիմիական արդյունքները պետք է լինեն կրթություն տրանս- գլիկոլներ ցիկլային էպոքսիդսը բաժանելիս: Իսկապես, ցիկլոֆեքսենսօքսիդի թթվային կատալիզացված հիդրոլիզի հետ կամ ցիկլոպենթենոքսիդը ձեւավորվում է բացառապես տրանս-1,2-դիոլ:

Այսպիսով, ալկեների էպոքսիդացման երկաստիճան գործընթացը, որին հաջորդում են էպօքսիդի թթու հիդրոլիզը, համապատասխանում է արձագանքին հակա- Ալկենեսի հիդրրոպիլիզացում:
Երկու փուլերը հակա- Ալկենը կարող է համակցվել, եթե ալկենը բուժվում է ջրով 30-70% ջրածնի պերօքսիդի հետ մրջյուն կամ տրիֆլորաաթթուով: Երկու այս թթուները բավականաչափ ուժեղ են, որպեսզի բուիրանի ցիկլի բացահայտումը պատճառի:

Հիմքի կողմից կատալիզացված Օքսիրանի օղակի բացահայտումը հանգեցնում է նաեւ ցիկլիկի ձեւավորմանը տրանս-Glikoli.

Հետեւաբար, Ալկալինի հետագա ալկալային հիդրոլիզացման հետագա ալկալային հիդրոլիզացման երկու փուլային գործընթացը նույնպես արձագանք է հակա- Ալկենեսի հիդրրոպիլիզացում:
3. կար-Հիդրոքսիլացիա
Օքսիդացման ամենաբարձր աստիճանում անցումային մետաղների որոշ աղեր եւ օքսիդներ արդյունավետ ռեակտիվներ են: կար- Alkenet- ի կրկնակի կապի հիդրօքսիզացումը, երբ երկու հիդրոքսիլային խմբերը միանում են երկակի կապի նույն կողմից: Ալկենեսի Permanganate կալիումի օքսիդացում - ամենահին մեթոդներից մեկը կար- Երկակի հաղորդակցության հիդրօքսիզացում. Շարունակվում է լայնորեն օգտագործվել, չնայած դրան բնորոշ սահմանափակումներին: ԱՊՀ-1.2-Cyclohexanediol- ը առաջին անգամ ստացավ V.V- ի կողմից: Markovnikov 1878-ին ցիկլոֆեսենի հիդրօքսիդացիայի միջոցով կալիումի պերմանգանատի ջրային լուծույթով 0 0 C- ում:

Ապագայում այս մեթոդը մշակվել է ռուս գիտնական E.E- ի աշխատանքներում: Wagner- ը, հետեւաբար կար- Ալկենեսի հիդրոպիլիզացումը Permanganate կալիումի ջրային լուծույթի գործողությամբ կոչվում է Վագների ռեակցիա: Կալիումի Permanganate- ը ուժեղ օքսիդացնող միջոց է, որը կարող է ոչ միայն հիդրոօսսի կրկնակի կապը, այլեւ բաժանվել է ձեւավորող Վիկինալ Դիոլը: Գլիպոլների հետագա մաքրումից խուսափելու համար անհրաժեշտ է ուշադիր հետեւել ռեակցիայի պայմաններին: Գլիկոլների ելքերը միաժամանակ սովորաբար փոքր են (30-60%): Լավագույն արդյունքները ձեռք են բերվում Ալկալինների թույլ ալկալային միջավայրում (PH ~ 8 9) 0-5 0-ով `KMNO 4-ի 1% ջրային լուծույթով նոսրացված:


Սկզբնապես, Ալկենեսի պերմանգանատ կալիումի օքսիդացման ժամանակ ձեւավորվում է մանգանաթթվի ցիկլային եթեր, որն անմիջապես հիդրոլցված է դեպի Վերեւյա Դիոլա:

Մանգանի թթվի ցիկլային Ester- ը որպես միջանկյալ չէր մեկուսացված, բայց դրա ձեւավորումը հետեւում է կալիումի պերմանգանատների պիտակավորվածներին. Երկու թթվածնի ատոմները պիտակավորված են, երբ Ալկինան օքսիդացում է 18-ով: Սա նշանակում է, որ եւ թթվածնի ատոմները շարժվում են օքսիդավորից, եւ ոչ թե լուծիչից `ջուրը, որը լավ է առաջարկվող մեխանիզմի համաձայն:
Մեկ այլ մեթոդ կար- Օսմիա օքսիդի (VIII) OSO 4-ի գործողությունների հիդրօքսիդիզացումը «Ռ. Կրիգան» առաջարկեց 1936 թ. OSMIA Tetraoxide- ը անգույն, թռչող, բյուրեղային, օդի, դիօքսանի, պիրիդինի եւ այլ օրգանական լուծիչների վրա լուծելի է: Երբ OSMIUM TETRAOXIDE- ը շփվում է օդում կամ դիօքսանում ալկանների հետ, ձեւավորվում է Osmumic թթու ցիկլային Ester- ի սեւ նստվածք `Օսմաթ, որը հեշտությամբ կարելի է մեկուսացնել անհատապես: OSO 4-ի երկակի պարտատոմսերի ավելացումը նկատելիորեն արագացվում է պիրիդինի լուծույթում: Օսաստտների տարրալուծումը դեպի վերեւում գլիկոլներ են ձեռք բերվում ջրային նատրիումի հիդրոզուլֆիտի կամ ջրածնի սուլֆիդի գործողությամբ:

Ապրանքի ելքեր կար-Հայենսի այս մեթոդով -yndroxylation- ը զգալիորեն բարձր է, քան Permanganate- ը որպես օքսիդացնող միջոց օգտագործելիս: Կրիգի մեթոդի կարեւոր առավելությունն է Ալկենեսի օքսիդացնող պառակտման արտադրանքների բացակայությունը, որը բնորոշ է Permanganate օքսիդացմանը:


OSMIA Tetraoxide- ը շատ թանկ եւ դժվարվող ռեակտիվ է, եւ այն թունավոր է: Հետեւաբար, OSMIA օքսիդը (VIII) օգտագործվում է փոքր քանակությամբ բարդ նյութերի սինթեզում `դիոլի բարձրագույն արդյունքը ստանալու համար: Պարզեցնելու համար կար-Հայոնեսի ոսպիոնների կողմից OSO 4-ի գործողությունների ներքո մշակվել է տեխնիկայով, որը թույլ է տալիս օգտագործել միայն այս ռեակտիվի կատալիտիկ քանակությունը: Alkene հիդրօքսիդավորումն իրականացվում է OSO 4-ի ներկայությամբ ջրածնի պերօքսիդի միջոցով, օրինակ.

Այս բաժնի ավարտից հետո մենք ստերոքիմիական հարաբերություններ ենք տալիս Ալկենի միջեւ ԱՊՀ- կամ տրանս- ձեւավորված Vical Diol- ի կազմաձեւում եւ կազմաձեւում, որը կարող է լինել ԱՊՀ- կամ տրանս-Այս, Էրրո- կամ Տականք-Ֆուդ Մեսո- կամ Դ, Լ.-Ֆորմ, կախված Alken- ի տեղակալներից.

Նման ստերեոքիմիական հարաբերություններ են նկատվում այլ ռեակցիաներում կար- կամ հակա- Hyd րածնի, հալոգենների, ջրի, հալոգենի, բորային հիդրացիների եւ այլ ռեակտիվների մատակարարման բազմակի ընթացքում:
Օրգանական նյութերի ներգրավմամբ վերափոխման ռեակցիաների հավասարումների կազմումը
Մեջ Ներկայացման հետ կապված հաղորդակցությունը, որպես մեկ պետական \u200b\u200bքննության բարձրագույն ուսումնական շրջանավարտների վերջնական սերտիֆիկացման միակ ձեւը եւ պրոֆիլային վերապատրաստման ավագ դպրոցի անցումը դառնում են ավելի ու ավելի կարեւոր է ավագ դպրոցի աշակերտների պատրաստմանը `առավելագույնը« թանկ » «Քիմիայի քննություն» փորձի «մասի» առաջադրանքները: Չնայած այն հանգամանքին, որ «C» -ի հինգ առաջադրանքները համարվում են տարբեր. Անօրգանական նյութերի քիմիական հատկություններ, օրգանական միացությունների փոխակերպման շղթաներ, հաշվարկված առաջադրանքներ. Բոլորը կապված են Redox ռեակցիաներ (OSR): Եթե \u200b\u200bOSR- ի տեսության հիմնական գիտելիքները սովորում են, ապա կարող եք ամբողջությամբ կատարել առաջին եւ երկրորդ խնդիրները ամբողջությամբ, իսկ երրորդը, մասնակի: Մեր կարծիքով, «C» - ը «C» -ին կատարելիս հաջողության զգալի մասը հենց դրանում է: Փորձը ցույց է տալիս, որ եթե ուսումնասիրում է անօրգանական քիմիան, ուսանողները լավ են դիմագրավվում OSR հավասարումների գրելու խնդիրներին, օրգանական քիմիայի նման առաջադրանքները նրանց մեծ դժվարություններ են առաջացնում: Հետեւաբար, օրգանական քիմիայի ամբողջ ընթացքի ընթացքում պրոֆիլային դասարաններում ուսումնասիրելու ընթացքում մենք փորձում ենք բարձր դասընթացի ուսանողների մոտ ձեւավորել OPR հավասարումների հավաքագրման հմտություններ:
Անօրգանական եւ օրգանական միացությունների համեմատական \u200b\u200bբնութագրերը ուսումնասիրելիս մենք ուսանողներ ենք ներկայացնում օքսիդացման աստիճանը (C.O.) (օրգանական քիմիայի մեջ, առաջին հերթին ածխածնի) եւ դրա որոշման մեթոդներ.
1) միջին S.O- ի հաշվարկ: ածխածնի օրգանական նյութերի մոլեկուլում;
2) S.O- ի սահմանում: Յուրաքանչյուր ածխածնի ատոմ:
Մենք նշում ենք, թե որ դեպքերում ավելի լավ է օգտագործել մեկ կամ մեկ այլ եղանակ:
Հոդվածը հրապարակվել է «Գեո-ճարտարագիտություն» ընկերության աջակցությամբ, որը ներկայացնում է շուկայում արտադրանքը «Պրոկկրեսլա» ապրանքանիշի ներքո: Ընկերության շրջանակը - տարբեր սրահների համար աթոռների եւ աթոռների արտադրություն, վաճառք եւ տեղադրում: Աշխատակազմի եւ նրանց արտադրական օբյեկտների բարձր պրոֆեսիոնալիզմը թույլ է տալիս արագ եւ արդյունավետորեն իրականացնել ցանկացած աստիճանի բարդությունների նախագծեր: «Profkresla» ապրանքանիշի ներքո գտնվող բոլոր ապրանքները Եղեք տոնական աթոռներ, սպասասրահների սենյակներ կամ ուսումնական հաստատություններում գտնվող աթոռներ, տարբերակել ժամանակակից եւ էրգոնիկ ձեւավորումը, ինչպես նաեւ բարձր մաշվածությունը, ուժը եւ հարմարավետությունը: Կայքում կատալոգում ներկայացված ապրանքների հսկայական տեսականին Profkresla.ru- ում միշտ կարող եք ընտրել այն մոդելները, որոնք լավագույնս տեղին են ձեր ընկերությունում ընդունված կորպորատիվ ոճին: Եթե \u200b\u200bդուք դեռ ընտրության հետ կապված դժվարություններ ունեք, ընկերության փորձագետները միշտ պատրաստ են խորհուրդներ տալ, օգնեք որոշել մոդելի մասին, ապա տեղում պատրաստել բոլոր անհրաժեշտ չափումները եւ տեղադրումը:
Իմաստ «Ալկանա» թեմայի ուսումնասիրությունը ցույց է տալիս, որ օքսիդացման, այրման, հալոգենացիայի, նիտրիացիայի, ջրազրկման, տարրալուծման գործընթացներն առնչվում են Redox գործընթացներին: Այրման ռեակցիաների հավասարումներն ու օրգանական նյութերի տարրալուծումը գրելիս ավելի լավ է օգտագործել C.O- ի միջին արժեքը: Ածխածին. Օրինակ:
Մենք ուշադրություն ենք հրավիրում էլեկտրոնային հաշվեկշռի առաջին կեսին. S.O- ի կոտորակային արժեքի ածխածնի ատոմում: Դենոմինատորը 4 է, ուստի էլեկտրոնների փոխանցման հաշվարկն իրականացվում է ըստ այս գործակիցի:
Այլ դեպքերում, «Ալկաններ» թեման ուսումնասիրելիս մենք որոշում ենք S.O- ի արժեքները: Միացության յուրաքանչյուր ածխածնի ատոմ, ուսանողների ուշադրությունը սեւեռելով առաջնային, միջնակարգ, երրորդային ածխածնի ատոմներում ջրածնի ատոմների փոխարինման հաջորդականությանը.


Այսպիսով, մենք ամփոփում ենք ուսանողներին այն եզրակացության մեջ, որ երրորդականում փոխարինման գործընթացը, ապա երկրորդային, եւ, վերջին անգամ `առաջնային ածխածնի ատոմներում:
Իմաստ «Ալկենես» թեմայի ուսումնասիրությունը հաշվի է առնում օքսիդացման գործընթացները, կախված Ալկենետի կառուցվածքից եւ ռեակցիոն միջավայրից:
Երբ ալկենները օքսիդացվում են կալիումի permanganate kmno 4-ի խտացված լուծույթով, թթվային միջավայրում (կոշտ օքսիդացում), տեղի է ունենում ընդմիջում, եւ - Carboxylic թթուների (IV) ձեւավորմամբ: Այս արձագանքը օգտագործվում է կրկնակի պարտատոմսերի դիրքը որոշելու համար:
Եթե \u200b\u200bկրկնակի պարտատոմսը մոլեկուլի վերջում է (օրինակ, Bouthena-1- ում), օքսիդացման արտադրանքներից մեկը ձեւավորաթթու է, հեշտությամբ օքսիդացված է ածխաթթու գազի եւ ջրի վրա.

Մենք շեշտում ենք, որ եթե Ալկինի մոլեկուլում կա ածխածնի ատոմ կրկնակի պարտատոմսով երկու ածխածնի փոխարինիչ (օրինակ, 2-մեթիլբուտեն -2 մոլեկուլում), այն ժամանակ, երբ այն օքսիդացում է, քանի որ դա օքսիդացում է, քանի որ փոխարկումը տեղի է ունենում Նման ատոմի մեջ կարբոքսիլ խմբի ատոմը անհնար է առանց C-C-Community- ի կոտրելու, այս պայմաններում համեմատաբար կայուն է.

Մենք նշում ենք, որ եթե ալկինի մոլեկուլը սիմետրիկ է, եւ երկակի կապը պարունակվում է մոլեկուլի մեջտեղում, օքսիդացման ժամանակ ձեւավորվում է միայն մեկ թթու:

Տեղեկացնում ենք, որ Ալկենեսի օքսիդացման առանձնահատկությունը, որի դեպքում կրկնակի պարտատոմսերով ածխածնի ատոմները կազմում են երկու ածխածնի արմատականներ, երկու Կետոնների ձեւավորումն է.


Հաշվի առնելով չեզոք կամ թույլ ալկալային լրատվամիջոցներում Ալկենեսի օքսիդացումը, կենտրոնացնելով ավագ դպրոցի աշակերտների ուշադրությունը այն փաստի վրա, որ նման պայմաններում օքսիդացումը ուղեկցվում է դիիչների ձեւավորմամբ, եւ հիդրոքսիլային խմբերը միանում են ածխածնի ատոմների ձեւավորմամբ , որի միջեւ կա կրկնակի կապ:

Մեջ Նմանապես, մենք համարում ենք ացետիլենայի եւ նրա հոմոլոգիաների օքսիդացումը, կախված այն բանից, թե ինչ է ընթանում շրջակա միջավայրը: Այսպիսով, մենք նշում ենք, որ թթվային միջավայրում օքսիդացման գործընթացը ուղեկցվում է Carboxylic թթուների ձեւավորմամբ.

Արձագանքը օգտագործվում է օքսիդացման ապրանքների ալկինների կառուցվածքը որոշելու համար.

Չեզոք եւ ցածր ալկալային լրատվամիջոցներում ացետիլենի օքսիդացումը ուղեկցվում է համապատասխան օքսիայի ձեւավորմամբ (օքսիդաթթվի աղեր), եւ հոմոլոգների օքսիդացումը եռակի պարտատոմսերի խզում է.

Մեջ ԵԽ կանոններն իրականացվում են ուսանողների հետ հատուկ օրինակներով, ինչը հանգեցնում է դրանց ավելի լավ կլանման տեսական նյութի: Հետեւաբար, տարբեր միջավայրերում ասպարեզի օքսիդացում ուսումնասիրելիս ուսանողները կարող են ինքնուրույն ենթադրել, որ թթվային ձեւավորումը պետք է սպասվի թթվային միջոցի մեջ, իսկ ալկալային աղերի մեջ: Ուսուցիչը միայն հստակեցվելու է, թե որ ռեակցիայի արտադրանքները ձեւավորվում են, կախված համապատասխան ասպարեզի կառուցվածքից:
Showing ուցադրվում է այն օրինակների վրա, որ մեկ կողմնակի շղթայով բենզոլի գոմոլոգները (անկախ դրա երկարությունից) օքսիդացվում են ածխածնի ատոմի կողմից բենզոիկաթթվի ուժեղ օքսիդացնող միջոցով: Գոմցոլի հոմոլոգիան օքսիդացվում է կալիումի պերմանգանատով չեզոք միջավայրում `բույր թթուների կալիումի աղեր ձեւավորելու համար:
5C 6 H 5 -CH 3 + 6KMNO 4 + 9H 2 SO 4 \u003d 5C 6 H 5 COOH + 6MNSO 4 + 3K 2 SO 4 + 14H 2 O,
5C 6 H 5 -C 2 H 5 + 12KMNO 4 + 18H 2 SO 4 \u003d 5C 6 H 5 COOH + 5CO 2 + 12MNSO 4 + 6K 2 SO 4 + 28H 2 O,
C 6 H 5 -CH 3 + 2kmno 4 \u003d C 6 H 5 Cook + 2mno 2 + Koh + H 2 O.
Մենք շեշտում ենք, որ եթե մոլեկուլում կան մի քանի կողմնակի ցանցեր, ապա թթվային միջավայրում, նրանցից յուրաքանչյուրը օքսիդացվում է Carboxyl խմբի A-Carbybend Aratic թթուների համաձայն:

Իմաստ OSR- ի հավասարումները կազմելու համար նախատեսված հմտություններ `ածխաջրածինների հավասարումները կազմելու համար թույլ են տալիս օգտագործել դրանք« թթվածնի պարունակող միացություններ »բաժինը ուսումնասիրելիս:
Այսպիսով, «Ալկոհոլը» թեման ուսումնասիրելիս ուսանողներն ինքնուրույն կազմում են ալկոհոլային օքսիդացման հավասարումները, օգտագործելով հետեւյալ կանոնները.
1) Առաջնային ալկոհոլները օքսիդացվում են Ալդեհիդների համար
3CH 3 -CH 2 OH + K 2 CR 2 O 7 + 4H 2 SO 4 \u003d 3CHO 3 -CHO + K 2 SO 4 + CR 2 (SO 4) 3 + 7 O;
2) երկրորդային ալկոհոլները օքսիդացվում են ketones- ին

3) Երրորդային ալկոհոլների համար օքսիդացման ռեակցիան բնութագիր չի:
Քննությանը նախապատրաստվելու համար ուսուցիչը խորհրդականորեն լրացուցիչ տեղեկություններ է տալիս նշված հատկություններին, ինչը, անկասկած, օգտակար կլինի ուսանողների համար:
Կալիումի պերմանգանատի կամ կալիումի ջրհեղեղի թթվայնացված լուծույթով մեթանոլի օքսիդացումով ձեւավորվում է CO 2-ը, առաջնային ալկոհոլները օքսիդացման ժամանակ, կախված արձագանքի պայմաններից, բայց նաեւ թթուներ: Օրինակ, ցուրտ ծայրերով էթանոլի օքսիդացում `սառնասրտությամբ, քացախաթթվի գոտիով, իսկ երբ ջեռուցվում է - Acetaldehyde:
3CH 3 -CH 2 OH + 2K 2 CR 2 O 7 + 8H 2 SO 4 \u003d 3CH 3 -COOH + 2K 2 SO 4 + 2CH 2 O,
3CH 3 -CH 2 OH + K 2 CR 2 O 7 + 4H 2 SO 4 3CHO 3 -CHO + K 2 SO 4 + CR 2 (SO 4) 3 + 7H 2 O.
Մենք կրկին հիշեցնում ենք ուսանողին ալկոհոլային օքսիդացման ռեակցիաների արտադրանքի վրա, մասնավորապես. KMNO 4-ի թեժ լուծումը `կաթնաշոռով ածխաթթուների եւ մնացած ալկոհոլային թթուների աղերը.

«Ալդեհիդներ եւ Քեթոններ» թեման ուսումնասիրելիս շեշտում են ուսանողների ուշադրությունը այն փաստի վրա, որ ալդեհիդները ավելի հեշտ են, քան ալկոհոլները, օքսիդացված համապատասխան կարբոքսային թթուների մեջ, ոչ միայն ուժեղ օքսիդացնող գործակալների (KMNO 4 եւ K- ի թթվածին, թթվածին, թթվածին, թթվածին, թթվածին, թթվածնի, թթվածին, թթվածին, օդային, թթվածին, օդգնացվող լուծումներ) 2 CR 2 O 7), բայց եւ թույլ կողմի ազդեցության տակ (ամոնիակ արծաթե օքսիդի կամ պղնձի հիդրօքսիդի (II)).
5CH 3 -CHO + 2KMNO 4 + 3H 2 SO 4 \u003d 5CH 3 -COOH + 2MNSO 4 + K 2 SO 4 + 3H 2 O,
3CH 3 -CHO + K 2 CR 2 O 7 + 4H 2 SO 4 \u003d 3CH 3 -COOH + CR 2 (SO 4) 3 + 2 SO 4 + 4H 2 O,
CH 3 -Cho + 2OH CH 3 -COONH 4 + 2AG + 3NH 3 + H 2 O.
Հատուկ ուշադրություն է դարձվում մեթանայի օքսիդացմանը `արծաթե օքսիդի ամոնիակ լուծույթով, քանի որ Այս դեպքում ձեւավորվում է ամոնիումի կարբոնատը, եւ ոչ թե ձեւավորված թթու.
Hchex + 4oh \u003d (NH 4) 2 CO 3 + 4ag + 6N 3 + 2H 2 O.
Որպես մեր երկար տարիների փորձը ցույց է տալիս, ավագ դպրոցի աշակերտների ուսման առաջարկվող մեթոդաբանությունը `օրգանական նյութերը ներգրավելու համար ORP հավասարումները կազմելու համար, քիմիայի մեջ քննության վերջնական արդյունքը մեծացնում է:
Alkenes Permanganate կալիումի օքսիդացումը `ջեռուցման ժամանակ ալկալային միջավայրում (կոշտ պայմաններ) հանգեցնում է նրանց ածխածնի կմախքի ոչնչացմանը երկակի կապի վայրում: Միեւնույն ժամանակ, կախված է վինիլային բեկորների հետ կապված ալկիլային խմբերի քանակից, կարելի է ձեռք բերել երկու կարբինգիկ \u200b\u200bթթուներ, թթու եւ քիթոն կամ երկու կետոններ.
UPR.11.Ինչ ապրանք է ձեւավորվում ցիկլոֆեքսենի օքսիդացման ժամանակ, կալիումի պերմանգանատի լուծույթը ցուրտ եւ (բ) խտացված կալիումի պերմանգանատանի լուծույթով `հետագա թթվայնացման միջոցով:
UPR.12.Ինչ ապրանքներ են ձեւավորվում 1,2-դիմեթիլկլոհեքսից `իր (ա) կատալիտիկ ջրածինացմամբ, (բ) կալիումի մշտական \u200b\u200bկալիումի պերմանգանատի օքսիդացում ցրտից, (գ) օզոնացիա` հետագա նվազող պառակտման միջոցով:
6.5. Էթիլենային օքսիդացում Acetaldehyde- ում
Էթիլենային օդային թթվածնի օքսիդացումը պալադիումի քլորիդների (II) եւ պղինձ (II) հանգեցնում է ացետալդեհիդի ձեւավորմանը ( Wheaker գործընթաց):
 (63)
(63)
Էթանալ (ացետալդեհիդ)
6.6. Քլորոզիզացնող էթիլեն
Վինիլային քլորիդը ձեռք է բերվում քլորոգենե էթիլենով.
6.7. Օքսիդացնող ամոնոլիզ
Ածխաջրածինների օքսիդացումը օդային թթվածնի միջոցով ամոնիակի ներկայությամբ հանգեցնում է ցիանո խմբում մեթիլ խմբի վերափոխմանը: Նման օքսիդացումը կոչվում է օքսիդացնող ամոնոլիզ: Ակրիլոնիտրիլը ձեռք է բերվում պրոպիլենի օքսիդացումով:
Ակրիլոնիտրիլ
Մեթանի օքսիդացնող ամոնոլիզը ձեռք է բերվում սինիլաթթու միջոցով.
 (66)
(66)
7. Ալկենեսի հիդրավլիկ (Oxosynthesis)
30-ից 250-ը 30-ից ջերմաստիճանում եւ 100-400 բանկոմատների ճնշում: Dicobaltoktacarbonyl- ի ներկայությամբ Ալդեհիդների ձեւավորմամբ Ալդեհիդների ձեւավորմամբ Ալդեհիդների ձեւավորմամբ Ալդեհիդների ձեւավորմամբ միանում են ջրածնի եւ ածխածնի երկօքսիդը: Isomers- ի խառնուրդը սովորաբար ձեռք է բերվում.
Մեխանիզմ.
1. Լիգայի ձեւավորում
2. Կցորդական էթիլեն

3. Էթիլենի ներդրումը

4. Կցելով Լիգան
5. CO- ի իրականացում
6. Օքսիդացուցիչ ջրածնի հավելված

7. Վերականգնման պիկապ

8. Carbnes- ի եւ Carbenoids- ի անդամակցությունը
Վերջին տարիներին օրգանական քիմիայի մեջ մեծ ուշադրություն է վճարվում Բենլենտ ածխածնի - կարբենների միացություններին: Խնձորների մեծ մասը անկայուն է եւ դրանց ձեւավորումից անմիջապես հետո արձագանքում են այլ կապերով:
8.1. Կարբենովի կառուցվածքը
Աննկատ կարբեն. CH 2, որը նույնպես կոչվում է մեթիլեն, կարող է լինել սինգլ կամ եռակի ձեւով: Carben- ի Singlet- ի տեսքով, զույգ անվերջ էլեկտրոնային էլեկտրներ, որոնք ունեն զույգ երկու պտույտներ, նույն ուղեծրով, մինչդեռ եռակի տեսքով, զուգահեռ պտույտներով երկու չպատրաստված էլեկտրոններ տեղակայված են նույն էներգիայի երկու ուղեղներով: Singlet- ի եւ Triplet Carbenes- ի տարբեր էլեկտրոնային կազմաձեւերը արտացոլվում են ինչպես այս մասնիկների տարբեր երկրաչափության մեջ, այնպես էլ տարբեր քիմիական գործունեության մեջ: Բռնալից ածխածնի ածխածնի ատոմը գտնվում է SP 2-հիբրիդային վիճակում, երկու էլեկտրոնները տեղակայված են SP 2-Flexidal Orbitals- ում (ալիք), իսկ P- orbo) անվճար է: Triplet Carben- ը բնութագրվում է Բենթ-ածխածնի SP-Hybridization- ով. Միեւնույն ժամանակ, երկու չպատրաստված էլեկտրոններ տեղակայված են երկու p-orbitals- ում, այսինքն, Եռիպտեան կարբենը կենդանի է: Singlet Methylene- ի համար H-H - H անկյունը, ըստ սպեկտրային տվյալների, 102-105 0 է, իսկ Triplet Methylene- ի համար, այս անկյունը մեծանում է մինչեւ 135140 օ: Սա համապատասխանում է Triplet Methylene- ի ավելի բարձր կայունությանը: Ըստ քվանտային մեխանիկական հաշվարկների, Triplet Methylene- ը իսկապես 10 կկալ / մոլ է ավելի կայուն սինգլ մեթիլեն:

Սակայն փոխարինողները, սակայն, ածենների այս երկու ձեւերի հարաբերական կայունության փոփոխություն են առաջացնում: Dialkyl Carben- ի համար եռակի ձեւը նույնպես ավելի կայուն սինգլ է, բայց Digalokarben- ի համար : Chal 2-ը եւ այլ Carbnes ունեցող փոխարինողներ, որոնք պարունակում են ջրված զույգ էլեկտրոններ, հիմնական պետությունը սինգլ է: Dichlorkarbena- ի C1-C-C1- ի արժեքի անկյունը, որը հավասար է 106-ի, լավ համահունչ է սինգլ ձեւի հետ: Digalocarbens- ի սինգլ ձեւի ավելի բարձր կայունություն `համեմատած եռակի հետ, ըստ երեւույթին, դրա կայունացման պատճառով` գոլորշու զույգի էլեկտրահեռականի հետ

Դիոկարբենի եռյակի ձեւի նման կայունացումը անհնար է: Ըստ քվանտային մեխանիկական հաշվարկման տվյալների, SoMlet- ի էներգիան `Dichlorkarben- ի եռյակի անցումը 13,5 կկալ / մոլ:
Ա. Դիչլորկարբեն
Դիգալոկարբենովը ստեղծելու համար մշակվում են ուժեղ հիմքերի ակցիայի համաձայն հալոգենային գեներից հալոգեն հիդոգենային գեներից հալոգեն հիլյի գեղարվեստական \u200b\u200bռեակցիայի արձագանքման վրա: Այս մեթոդը պատմականորեն առաջինն էր, որի օգնությամբ Կարբենովից առաջինը ստեղծվեց որպես միջանկյալ - Դիչլորկարբեն (J .. Hein 1950): Քլորոֆորմի ծանր հիմքերի հետ շփվելիս (RKA քլորոֆորմ ~ 16), BromOormal (RCA \u003d 9) եւ այլ տերմայնաչափեր ձեւավորվում են անիոն, որը կայունանում է, վերացնելով Հալոկարբենի ձեւավորմամբ: Ուժեղ հիմքերի քլորոֆորմի գործողությունը ստացվում է Դիչլորկարբենին.
dichlorkarben
Որպես հիմք, կարող են օգտագործվել նաեւ անտարբեր ատիկ միջավայրում լիտրիումիգանային միացություններ: Այնուհետեւ -100 0 C- ն կարող է ամրագրվել Trichloromethyl Lithium- ի ձեւավորման մեջ `որպես միջանկյալ:

Օգտագործելով ուժեղ հիմքեր, ինչպիսիք են RLI- ն, կարող եք ստեղծել կարբերված 1,1-Digalognesis ածանցյալներից

Վերջին տարիներին, փոխարենը Digalokarben- ը առաջացնելու համար Ն.-Բյութիլիտիան լայնորեն օգտագործվում է որպես BIS (Trimethylsilyl) նատրիումի հիասքանչ:
Միեւնույն ժամանակ, առանձնանում է քիմիապես իներտ, սիրող [BIS (Trimethylsilyl) Amide]: BIS (Trimethylsilyl) նատրիումի Amide- ը, ի տարբերություն N-Butyl Lithium- ի, կարող է առանձնացվել իներտ մթնոլորտում `չոր ձեւով: Գործնականում, դրա հիմնական լուծումները կարող են օգտագործվել ավելի հաճախ, որը երկար ժամանակ կարող է պահվել սենյակային ջերմաստիճանում:
Dichlorkarben- ը կարող է առաջանալ նաեւ նատրիումի չոր քլորոակեետատի ջերմային ապամոնտաժով.
Նատրիումի հիդրօքսիդի գործողության ներքո քլորոֆորմից Dichlorkarbena արտադրելու ամենա մատչելի ժամանակակից մեթոդներից մեկը մանրամասն նկարագրվելու է ավելի ուշ:
Dichlorkarben- ը միանում է ալկեններին, տալով Dichlorocyclopropans- ին: Կապը տեղի է ունենում Ստերերետեկի - նախնական ալկենի կազմաձեւը պահպանվում է ռեակցիայի արտադրանքի մեջ - Cyclopropane:
 (69)
(69)
տրանս-2-բան տրանս-1,2-dimethyl-3,3-
dichlorcyclopropan
 (70)
(70)
ԱՊՀ-2-բան Գ.դեպի-1,2-dimethyl-3,3-
dichlorcyclopropan
 (71)
(71)
7,7-dichlorubicloheptan
Լիթիումի գործողության ներքո 1,1-ը դիլոկիկլոկրոպները վերականգնելիս mPEM-Բութիլ ալկոհոլը, ցինոտաթթու կամ նատրիումի հեղուկ ամոնիակում եւ հալոգեն ատոմները փոխարինվում են ջրածնիով: Սա ցիկլոպրոպային ածանցյալների արտադրության ընդհանուր մեթոդներից մեկն է:
Հեծանվորդ:
UPR տասնմեկ.Լրացրեք արձագանքը.


(Z) -3-մեթիլ-2-պենտենե մեթիլենեկիկլոհեքսան
Պատասխան

Բ. Մեթիլեն
Methylene- ը կարելի է ձեռք բերել դիազոմեթանի տարրալուծմամբ: Diazomethane- ը համեմատաբար անկայուն նյութ է, որը քայքայվում է ազոտի եւ մեթիլենի ճառագայթահարումը:
 (73)
(73)
Դիազոմետան
Methylene. CH 2 դիազոմեթանի ֆոտոլիդիով ձեւավորվում է ավելի քիչ կայուն սինգլ ձեւով: Singlet Methylene- ը դիազոմեթանի կամ ազոտի մոլեկուլների բախումների արդյունքում արձագանքման պայմաններում, այն արագորեն կորցնում է էներգիան եւ վերածվում ավելի կայուն եռյակի մեթիլենի:
Singlet Carbenis- ի համար այն բնութագրվում է սինխրոն կապով Ալկենի կրկնակի կապի հետ երկակի կապի մեջ գտնվող երկրաչափության ամբողջական պահպանմամբ (ռեակցիա - ցիկլոպեր): Կրկնակի պարտատոմսերի համար կարբենիի սինգլ ձեւի կցորդը տեղի է ունենում, այսպիսով, խստորեն ստերեետեկը:
B. Արագություն Simmons-Ձի
Հիլոկրոպային ածանցյալներում Ալկրոնական ածանցյալներում Ալկրոնական ածանցյալների վերափոխման շատ պարզ մեթոդը հիմնված է Ալոդիստական \u200b\u200bմեթիլենի եւ ցինկի եւ պղնձի խառնուրդի հետ Ալկենեսի արձագանքի վրա: Այս արձագանքը բացվել է 1958-ին, Սիմոնս եւ Սմիթ եւ անմիջապես շահել լայն հանրաճանաչություն ցրադարձային ածանցյալների սինթեզում: Այս արձագանքի ակտիվ մասնիկը կարբեն չէ : CH 2, իսկ Carbenoid - Iodide Iodomethyl հեծանվավազքը Iznch 2 I- ն, որը ձեւավորվել է մեթիլենային յոդիդի եւ ցինկի-պղնձի զույգի փոխազդեցությամբ:
diiodmethane Iodomeomethylcinodide
(Իրական Simmons Smith)
 (75)
(75)
Արձագանքը անցնում է հետեւյալ մեխանիզմով.

Simmons Smith Reaction- ը Ալկլոպրոուում Ալկրոնականը փոխարկելու շատ հարմար մեթոդ է:
UPR 12.Լրացրեք արձագանքը.


Պատասխան
 (76)
(76)
methylenecyclopentan Spiropeptan.
 (77)
(77)
styrene Cyclopropylbenzene.
 Ավարտել. Կահույք: Վերանորոգում: Տեղադրում Ընտրություն: Բացում
Ավարտել. Կահույք: Վերանորոգում: Տեղադրում Ընտրություն: Բացում